今年以来,565net必赢官方网谭志凯教授课题组在Biofabrication,Bio-Design and Manufacturing等生物制造相关期刊上新发表了一系列研究成果。
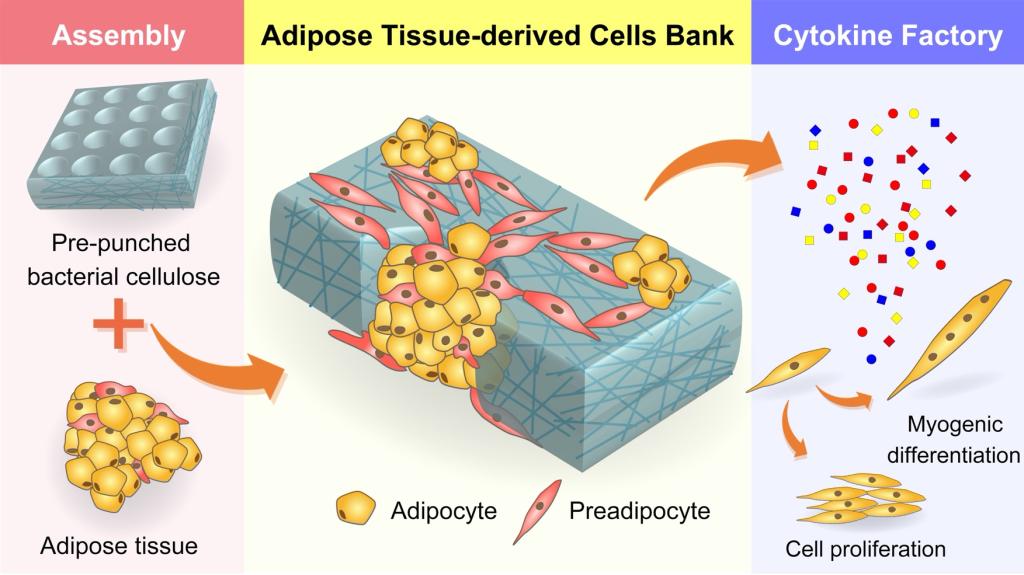
开发适合于体外培养的脂肪模型能为组织修复、代谢疾病及相关的研究提供助力。常规的通过二维平面培养建立的脂肪模型需要额外添加化合物以诱导脂肪细胞的成熟,这种方法较为复杂且大大增加了工业化生产的成本。谭志凯团队在“In vitroadipogenesis and long-term adipocyte culture in adipose tissue derived cell banks”一文中提出了一种采用多孔3D支架建立脂肪模型的方法。通过将分离的脂肪组织接种到合适的支架后,不仅能促进前脂肪细胞的黏附、增殖和成脂分化,而且有助于前脂肪细胞发生显著的自发脂质积累。利用该方法建立的组织来源的脂肪细胞库能够分泌大量促进成纤维细胞增殖和成肌细胞分化的细胞因子,在脂肪重建以及肌肉修复中都具有很大的应用潜力。相关研究成果发表在杂志Biofabrication上(DOI:10.1088/1758-5090/ac0610)。硕士研究生陈昊翔和王小成为论文并列第一作者,谭志凯教授为该论文的通讯作者。
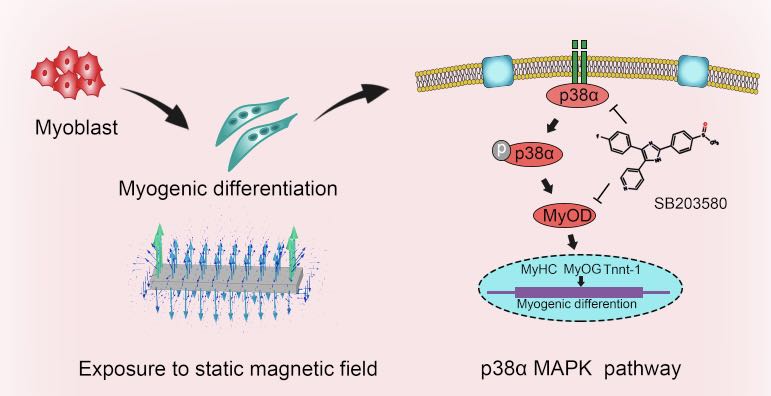
物理刺激,包括磁刺激和机械刺激,在细胞反应的调节中起着重要的作用。谭志凯团队在“Regulated skeletal muscle regeneration using 3D printed tissue repair patch”一文中,利用E-jet 3D打印技术制备了一种新型组织再生贴片,结合静态磁场,通过机械和磁刺激调控骨骼肌再生。该方法能诱导成肌细胞形成定向的多核肌管并通过激活p38 MAPK途径启动肌原性分化,是一种能够快速诱导受损骨骼肌组织再生的技术。相关研究成果发表在杂志Bio-Design and Manufacturing上,硕士研究生王小成为论文第一作者,谭志凯教授为该论文的通讯作者。
以上研究均通过生物智能制造手段,以组织器官系统再生、修复与重建为目标,为解决组织再生与器官移植等医学瓶颈提供了新助力!
通讯员:王小成
